玻璃显色原理与调控技术研究
彩色玻璃在建筑装饰、电子显示、光学器件等领域具有广泛应用,从哥特式教堂的彩绘玻璃窗到智能手机的渐变色后盖,其色彩呈现背后蕴含着复杂的物理化学机制。玻璃作为以硅酸盐为主要成分的非晶态固体,本身呈透明状,其色彩的产生是光与玻璃微观结构、化学成分相互作用的结果。本文将从颜色的本质属性出发,系统阐述玻璃显色的核心机制,并详解其颜色调控的关键技术手段。
一、颜色的科学本质:光、物体与视觉系统的协同作用
颜色并非物体固有的物理属性,而是可见光、物体材料、人类视觉系统三者共同作用产生的感知现象。要理解玻璃的显色原理,需先明确光的特性与颜色感知的基本规律。
(一)光的本质与可见光特性
光的本质是一种电磁波,具有波粒二象性,其能量传播以光子为载体。根据波长差异,电磁波可分为无线电波、红外线、可见光、紫外线等波段,其中能被人类视觉系统感知的“可见光”波段范围为400760纳米(对应频率375~750THz)。不同波长的可见光会引发不同的颜色感知:波长620750纳米的光被感知为红色,560590纳米为黄色,500560纳米为绿色,450480纳米为蓝色,400450纳米为紫色,各波长区间的过渡光则形成橙、青等中间色。
(二)颜色感知的三要素
物体的颜色由“光源照射物体选择性作用视觉系统接收”三个环节决定,缺一不可:
1.光源照射:提供具有特定波长分布的可见光,如太阳光为全光谱可见光,白炽灯以长波红光为主,荧光灯则包含较多短波蓝光;
2.物体选择性吸光:物体通过吸收、反射或透射特定波长的光,改变入射光的波长分布——玻璃作为透光材料,其颜色主要由“透射光的波长组成”决定,即玻璃吸收部分波长光后,剩余光透过并进入人眼;
3.观察者视觉系统:人眼视网膜中的视锥细胞感知可见光,通过视觉神经将信号传递至大脑,形成颜色认知。人类约能区分1000万种颜色,但感知结果受个体生理差异(如色弱、色盲)与环境因素(如背景色对比)影响,具有一定主观性。
(三)颜色的基本属性
颜色具有色相、明度、纯度三个核心属性,是描述玻璃色彩特征的关键指标:
色相:即色彩的类别,如红、绿、蓝等,由透过玻璃的可见光主波长决定;
明度:指颜色的明亮程度,与透过光的强度正相关,白色玻璃明度最高,黑色玻璃明度最低;
纯度(饱和度):指色彩的鲜艳程度,纯波长光形成的颜色纯度最高,混入其他波长光后纯度降低,如纯蓝色玻璃混入白光后会变为淡蓝色。
二、玻璃显色的四大核心机制
玻璃的显色源于其内部微观结构或化学成分对可见光的选择性作用,根据作用原理的差异,可分为离子选择性吸收、胶体粒子散射与吸收、电荷迁移跃迁、能带结构与本征吸收四类核心机制。
(一)离子选择性吸收机制:过渡金属离子的光吸收特性
该机制是工业生产中最常用的玻璃显色方式,核心是通过在玻璃原料中引入过渡金属离子(如Fe²⁺、Co²⁺、Mn³⁺、Ni²⁺等),利用其电子结构特性选择性吸收特定波长的可见光。
过渡金属离子的核外电子具有未充满的d轨道,当可见光照射时,电子可在不同能级的d轨道间发生跃迁,跃迁过程需吸收特定能量(对应特定波长)的光子。未被吸收的光子透过玻璃,形成与吸收光互补的颜色。典型案例包括:
钴离子(Co²⁺):电子跃迁吸收波长580620纳米的橙黄色光,透过光以蓝、紫波段为主,使玻璃呈现纯净的蓝色(即“钴蓝玻璃”);
二价铁离子(Fe²⁺):吸收400500纳米的蓝、紫波段光,透过光以绿、黄波段为主,玻璃呈绿色;
三价铁离子(Fe³⁺):吸收500600纳米的黄、绿波段光,透过光以红、蓝波段为主,玻璃呈浅黄色;
锰离子(Mn³⁺):吸收450550纳米的绿、蓝波段光,透过光以红、紫波段为主,玻璃呈紫红色。
(二)胶体粒子散射与吸收机制:纳米颗粒的光学效应
当玻璃内部形成尺寸与可见光波长(400760纳米)相近的纳米级胶体粒子(如金、银、铜等金属胶体)时,粒子会通过“光散射”与“表面等离子体共振”效应改变光的传播路径,进而使玻璃呈现颜色。
光散射效应:胶体粒子的尺寸与光波长相当,会导致光的传播方向发生无规则改变,散射强度与粒子尺寸、光波长密切相关——粒子尺寸越大,对长波长光的散射越强;
表面等离子体共振效应:金属胶体粒子表面的自由电子会与特定波长的可见光发生共振,导致该波长光的吸收强度显著增强。
典型案例为“金红玻璃”:当玻璃中分散直径50100纳米的金胶体粒子时,金粒子表面电子与500550纳米的绿、蓝光发生共振并强烈吸收,同时散射620700纳米的红光,最终玻璃呈现温暖的红色。此外,银胶体粒子可使玻璃呈黄色或棕色,铜胶体粒子则使玻璃呈红色或紫色,粒子的浓度与尺寸会进一步影响颜色的深浅与饱和度。
(三)电荷迁移跃迁机制:离子与配位体的电子交换作用
玻璃中的金属离子会与周围的“配位体”(如氧原子、氟原子等)形成稳定的配位结构,当电子在金属离子与配位体之间发生转移(即“电荷迁移”)时,需吸收特定波长的可见光以提供能量,从而使玻璃产生颜色。
该机制的核心是“配位环境对电荷迁移能量的影响”:金属离子的种类、价态及配位体的类型、数量,会决定电子转移所需的能量(对应光的波长)。以铁离子为例:在硅酸盐玻璃中,Fe³⁺与周围的氧原子形成[FeO₆]⁹⁻配位结构,电子从氧原子(低电势)向Fe³⁺(高电势)转移时,需吸收400450纳米的蓝光,剩余光透过玻璃后呈现浅黄色;若玻璃中引入氟离子(F⁻)替代部分氧原子,配位结构变为[FeO₄F₂]⁹⁻,电子转移所需能量降低,吸收波长红移至500纳米左右,玻璃颜色变为淡绿色。
(四)能带结构与本征吸收机制:玻璃材料的固有光学属性
从固体物理角度,玻璃的能带结构由“价带”(电子稳定存在的低能量带)、“导带”(电子可自由移动的高能量带)及两者之间的“禁带”(无电子存在的能量区间)组成。当光子能量大于禁带宽度时,价带电子会被激发至导带,该过程称为“本征吸收”,吸收的光子波长由禁带宽度决定(公式为λ=hc/Eg,其中h为普朗克常数,c为光速,Eg为禁带宽度)。
普通硅酸盐玻璃的禁带宽度约为56电子伏特(eV),对应吸收波长为200250纳米(属于紫外区),可见光可完全透过,故呈透明状。若通过原料改性(如引入硫化物、硒化物等半导体成分)缩小禁带宽度,本征吸收会延伸至可见光区,使玻璃呈现颜色:
含硫化镉(CdS)的玻璃禁带宽度约为2.4eV,本征吸收波长约为520纳米(绿光),透过光以红、蓝光为主,玻璃呈紫红色;
含硒化锌(ZnSe)的玻璃禁带宽度约为2.7eV,本征吸收波长约为460纳米(蓝光),透过光以红、绿光为主,玻璃呈黄色。
三、玻璃颜色的调控技术体系
工业生产中,需通过精准调控原料成分、熔制工艺参数及深加工处理,实现玻璃颜色的定制化与稳定性控制。
(一)原料成分调控:着色基础的精准配置
原料成分是决定玻璃颜色的核心因素,主要通过添加着色剂、调整澄清剂与助熔剂实现调控。
1.着色剂的选择与用量控制
着色剂以金属氧化物为主,需根据目标颜色选择对应的氧化物,并严格控制用量:
目标颜色为绿色时,添加氧化亚铁(FeO,提供Fe²⁺),用量通常为0.1%0.5%(质量分数),用量过高会导致颜色过深;
目标颜色为紫色时,添加氧化锰(MnO₂,高温下转化为Mn³⁺),用量为0.2%0.8%,用量过低则颜色偏浅;
目标颜色为蓝色时,添加氧化钴(CoO,提供Co²⁺),用量仅需0.01%0.05%,过量会使玻璃呈深蓝色甚至黑色。
2.澄清剂与助熔剂的间接调控作用
澄清剂(如三氧化二锑Sb₂O₃、硫酸钠Na₂SO₄)的作用是去除玻璃中的气泡,助熔剂(如碳酸钠Na₂CO₃、硼酸H₃BO₃)的作用是降低玻璃熔制温度,二者虽本身不着色,但会通过影响着色离子的价态与分布间接调控颜色:
三氧化二锑(Sb₂O₃)可与Fe³⁺发生氧化还原反应,将部分Fe³⁺还原为Fe²⁺,使玻璃颜色从浅黄色转为浅绿色;
硼酸(H₃BO₃)会改变玻璃的配位环境,使Fe³⁺的配位结构从[FeO₆]⁹⁻转为[FeO₄]⁵⁺,电荷迁移吸收波长红移,玻璃颜色加深。
(二)熔制工艺参数调控:颜色稳定性的关键保障
玻璃熔制过程的温度、时间、气氛三大参数,会直接影响着色离子的溶解、扩散及价态变化,进而影响颜色的均匀性与稳定性。
1.温度调控
熔制温度决定着色离子的溶解速率与胶体粒子的形成状态:
对于含金属胶体的玻璃(如金红玻璃),温度过低会导致胶体粒子聚集不均,颜色出现斑点;温度过高则粒子过度生长,散射效应增强,颜色变浅。通常需控制在14501550℃,确保粒子均匀分散(尺寸50100纳米);
对于含硒镉化合物的玻璃,温度升高会促进硒(Se)、镉(Cd)的扩散,使硒镉粒子(如CdSe)均匀分布,颜色更鲜艳,最佳温度为15001580℃。
2.时间调控
熔制时间影响玻璃的均化程度与着色离子的反应充分性:
时间过短:着色离子溶解不充分,玻璃出现颜色不均;
时间过长:易导致挥发性着色成分(如Se、CoO)流失,颜色变浅。例如,熔制钴蓝玻璃时,最佳时间为46小时,可确保Co²⁺均匀分散且无明显挥发。
3.气氛调控
熔制气氛(氧化气氛或还原气氛)通过改变着色离子的价态实现颜色调控:
氧化气氛:通入氧气(O₂)或空气,使着色离子向高价态转化,如Fe²⁺被氧化为Fe³⁺,玻璃从绿色转为浅黄色;
还原气氛:通入氢气(H₂)或一氧化碳(CO),使着色离子向低价态转化,如Fe³⁺被还原为Fe²⁺,玻璃从浅黄色转为绿色。工业中常用“天然气不完全燃烧”产生还原气氛,气氛的氧分压需精准控制(通常为10⁻⁶10⁻⁴atm)。
(三)深加工处理:颜色功能的拓展与优化
通过热处理、表面处理等深加工技术,可进一步调整玻璃颜色或赋予其特殊色彩效果。
1.热处理调控
对成型后的玻璃进行退火、淬火或晶化处理,通过改变内部结构影响颜色:
退火处理:缓慢降温(降温速率510℃/min)释放玻璃内部应力,同时促进着色离子的重新分布或微小晶体析出。例如,含氧化铈(CeO₂)的玻璃经400500℃退火后,会析出CeO₂微晶,微晶吸收450500纳米的蓝光,使玻璃呈暖黄色;
淬火处理:快速降温(降温速率>100℃/min)抑制晶体析出,使着色离子保持均匀分散状态,可避免颜色因晶体生长而变浅。
2.表面处理调控
通过镀膜、涂层等技术在玻璃表面形成光学功能层,赋予玻璃新的颜色特性:
薄膜干涉仪镀膜:在玻璃表面镀制单层或多层光学薄膜(如二氧化钛TiO₂、二氧化硅SiO₂),利用光的干涉效应改变透过光的波长分布。例如,镀制TiO₂/SiO₂多层膜的玻璃,在不同角度下会呈现蓝、紫、绿等渐变颜色(即“干涉色”),常用于手机后盖玻璃;
着色涂层:在玻璃表面涂覆含无机颜料(如氧化铁红、钴蓝)的涂层,直接赋予玻璃目标颜色,涂层厚度(通常为520微米)决定颜色深浅,该技术适用于大面积建筑玻璃。
四、彩色玻璃的应用演进与技术前沿
彩色玻璃的应用历史可追溯至公元前1500年的古代埃及(蓝色玻璃珠),中世纪欧洲的哥特式教堂将其推向艺术高峰(如巴黎圣母院的彩绘玻璃窗);进入现代,随着材料科学与工艺技术的进步,彩色玻璃的应用领域不断拓展:
建筑领域:用于幕墙玻璃、室内装饰玻璃,通过颜色调控实现采光与隔热的平衡;
电子领域:用于智能手机后盖、显示器玻璃,通过渐变镀膜、电致变色等技术提升外观与功能;
新能源领域:用于光伏玻璃,通过颜色调控(如浅棕色)提升对太阳光的吸收效率;
光学领域:用于滤光片、棱镜等光学器件,通过精准颜色控制实现特定波长光的筛选。
当前,彩色玻璃技术正朝着“多功能集成”方向发展,如:
电致变色玻璃:通过通电改变着色离子的价态,实现颜色与透明度的动态调控,适用于智能车窗、节能建筑;
光致变色玻璃:通过光照激发离子电子跃迁,实现颜色可逆变化,适用于防眩光眼镜、智能遮阳玻璃;
复合功能玻璃:结合颜色调控与抗菌、自清洁等功能,如含银离子的蓝色抗菌玻璃,适用于医疗场所。
玻璃的显色过程是光与物质相互作用的微观过程,其核心机制涵盖离子吸收、胶体散射、电荷迁移、能带吸收四类,而颜色调控则需通过原料、熔制、深加工的协同优化实现。从古代艺术品到现代高科技产品,彩色玻璃的发展不仅反映了人类审美需求的变迁,更体现了材料科学与工艺技术的进步。未来,随着微纳加工、智能控制等技术的融入,彩色玻璃将在更多领域发挥重要作用,为人类生活带来更丰富的色彩与功能体验。
-
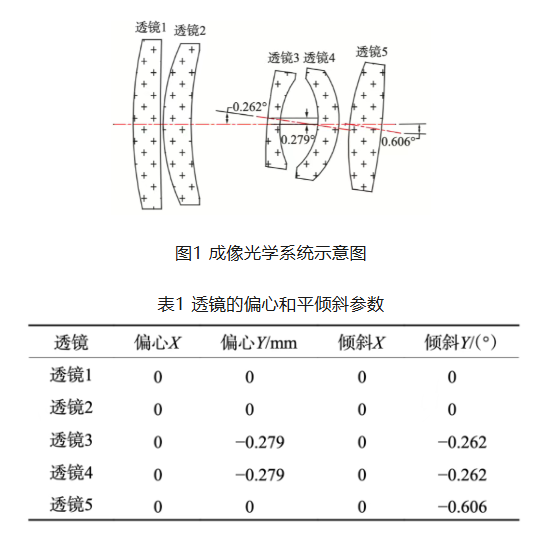
多基准轴透射式离轴光学系统高精度定心装调方法
星载光谱仪可获取空间连续分布的光谱数据,是陆地植被监测、海洋环境探测等领域的核心载荷。为校正分光系统引入的畸变,星载光谱仪成像透镜多采用离轴透射式设计,由此形成的多光轴结构存在大倾角、大偏心特征,超出了传统同轴系统定心装调方法的适用范围。本文提出一种多基准轴定心装调方法(Multi-referenceAxisAlignment,MAA),通过镜筒结构一体化加工预置各光轴的偏心与倾斜参数,结合光学平板实现基准轴的高精度引出,将复杂多光轴系统的装调拆解为多个单光轴子系统的独立装调,突破了传统定心仪的测量范围限制。针对某星载光谱仪3光轴离轴透射系统开展装调验证,实测结果表明,透镜最大偏心误差小于25.4μm,最大倾斜误差小于17.7″,系统实际畸变与理论值平均偏差小于0.32μm,全面满足设计指标要求。该方法为离轴折射类光学系统的高精度装调提供了可行的技术路径,拓展了透射式光学系统装调的适用边界。
2026-05-22
-
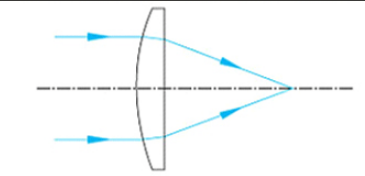
平凸透镜朝向对光束会聚效果及像差特性的影响分析
平凸透镜是各类光学系统中应用最为广泛的基础折射元件之一,属于典型的无限共轭透镜,核心光学功能分为两类:一是将点光源出射的发散光束准直为平行光束,二是将入射的准直平行光束会聚至单点。在激光光学、显微成像、光电检测等领域的光路设计与装调中,平凸透镜的安装朝向是直接影响系统性能的核心参数,其选择直接决定了像差水平与最终会聚效果。
2026-05-21
-
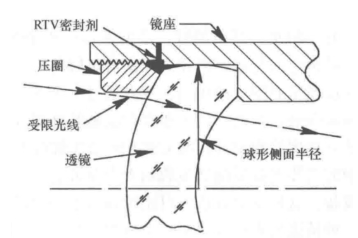
光机系统设计:镜头装配轴向预紧力计算(一)——通用设计原则与基础方法
本文基于光机系统设计领域的经典工程理论,系统阐述镜头装配中透镜面接触安装技术的核心原理,明确轴向预紧力在透镜固定、精度保持与环境适应性中的关键作用,详细介绍标称轴向预紧力的基础计算方法、参数定义与适用边界,同时解析轴向预载对透镜自动定心、抗径向偏心的力学效应,为光学镜头的装调设计提供标准化的工程参考。
2026-05-21
-
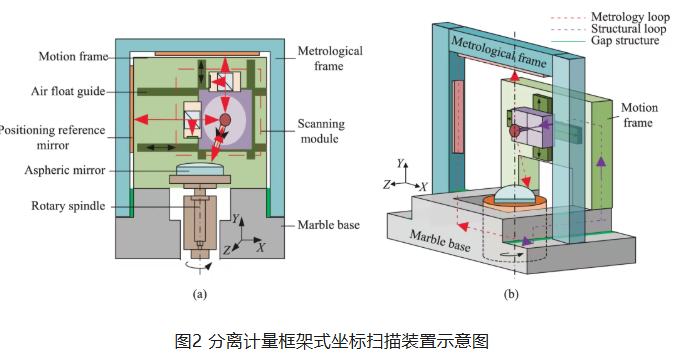
高精度轴对称非球面反射镜面形轮廓非接触式测量方法
非球面光学元件是高端光学系统的核心器件,其面形轮廓的高精度、可溯源测量是保障加工质量与系统性能的关键。本文针对轴对称非球面反射镜的测量需求,建立了通用化的非球面扫描轨迹数学模型,提出一种基于独立计量回路的非接触式坐标扫描测量方法。该方法采用运动与计量分离的框架结构,有效隔离运动误差对测量结果的影响;测头采用集成阵列式波片的四象限干涉测量系统,实现1nm级测量分辨率;通过扫描执行机构与多路激光干涉系统共基准设计,实现测量值可溯源至“米”定义。试验验证表明,该方法测量误差小于0.2μm,重复性精度达70nm,整体测量精度达到亚微米级,为非球面测量的量值统一与溯源提供了成熟的技术方案。
2026-05-21
-

麻省理工学院固态激光雷达硅光子芯片核心突破解读
麻省理工学院研究团队攻克了硅光子集成光学相控阵(OPA)固态激光雷达的长期核心瓶颈,通过创新的低串扰集成天线阵列设计,首次实现了宽视野扫描+低噪声高精度的无活动部件激光雷达芯片,为下一代紧凑、高耐用性固态激光雷达的落地奠定了技术基础。
2026-05-20








